INDICE DE CARACTERÍSTICAS
Características de las reacciones químicas
Cambia la composición de las sustancias obtenidas
 La composición del producto de la reacción química no es igual a la composición inicial del reactivo. Al formarse nuevas sustancias las propiedades del mismo cambian. Un ejemplo es el producto de un gas al hacer efervescencia una sustancia; el cambio de color y la aparición de calor en un producto QUIMICO
La composición del producto de la reacción química no es igual a la composición inicial del reactivo. Al formarse nuevas sustancias las propiedades del mismo cambian. Un ejemplo es el producto de un gas al hacer efervescencia una sustancia; el cambio de color y la aparición de calor en un producto QUIMICO
Una de las mejores formas de reconocer una reacción química es al observar cambios en la consistencia de este.
Reversibles e irreversibles
Las reacciones químicas pueden ser tanto reversibles como irreversibles. Reversibles, en caso de que en la reacción los productos pueden regresar a ser reactivos y serán irreversibles si en la reacción los productos no regresan a ser las sustancias reactivas iniciales. Por ejemplo, la combustión de un producto es una reacción INRREVERSIBLES
Cambian los átomos de estructura
Al ocurrir una reacción química, los átomos o iones que componen una sustancia continúan siendo los mismo, sin embargo, cambia la forma de enlace entre ellos. Al romperse los enlaces químicos de los reactivos iniciales, crean nuevos enlaces los cuales conforman los nuevos productos como resultado de la reacción química. Es diferente al tratarse de reacciones nucleares, donde las alteraciones se llevan a cabo en la estructura nuclear.
Ocurren en su mayoría en un medio acuoso
Muchas de las reacciones químicas suceden entre iones y moléculas disueltas en agua, que es el disolvente universal, o también en otros tipos de disolventes. Las moléculas se mezclan al ser disueltas de manera uniforme en un disolvente.
Simples y complejas
Cuando basta únicamente con un paso para que la sustancia original o reactivo se transforme en el producto, la reacción será simple, por otra parte, cuando sean necesarios varios pasos para que el reactivo se convierta en producto, la reacción será compleja. También se da el caso de que entre los pasos que conforman el proceso de reacción, se formen compuestos que no son reactivos ni tampoco productos, sino que son mediadores.
Igual cantidad de átomos
 En una reacción química el número de átomos del reactivo será igual al número de átomos del producto. Esto se fundamenta en la ley de la conservación de materia o ley de Lomonósov-Lavoisier, esta ley afirma que la cantidad de materia antes y después de una transformación química permanecerá siempre invariable.
En una reacción química el número de átomos del reactivo será igual al número de átomos del producto. Esto se fundamenta en la ley de la conservación de materia o ley de Lomonósov-Lavoisier, esta ley afirma que la cantidad de materia antes y después de una transformación química permanecerá siempre invariable.
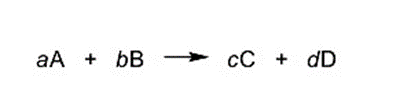
Es necesario que tener esta ley en cuenta al momento de escribir la ecuación química, para que la ley se cumpla será necesario acomodar la ecuación, para que haya un balance. Los números estequiométricos estarán frente a cada molécula en el índice, estos multiplicarán los átomos de la sustancia.
Energía
Durante las reacciones químicas, además de haber transformaciones en sus propiedades y componentes, ocurrirán transformaciones energéticas. Cuando una reacción química emite energía, esta será una reacción exotérmica, sin embargo, si la energía es absorbida en la reacción química, será una reacción endotérmica.
Es de gran ayuda la aplicación de la termodinámica en la química, encargada del estudio de las transformaciones de energía en la reacción química, para poder determinar si es posible la realización del proceso de reacción, sin tener que llevarlo a cabo.
No hay comentarios:
Publicar un comentario